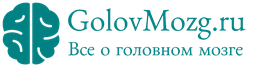Последствия гипоксии, которая сопровождается дефицитом кислорода в тканях головного мозга, у новорожденных связаны с нарушениями, вызванными кислородным голоданием. Расстройство оксигенации мозгового вещества приводит к метаболическим сбоям, в частности к нарушению процессов окисления, развитию ацидоза (смещение кислотно-щелочного баланса в сторону увеличения кислотности), уменьшению энергетического клеточного потенциала, избытку нейромедиаторов, нарушению обмена веществ в нервной ткани – в глиальных клетках и нейронах.
Характеристика патологии
Гипоксия мозга – недостаток снабжения мозгового вещества кислородом, патология у новорожденного часто приводит к серьезным нарушениям физического и психического развития. Перинатальная (возникающая в период с 22 недели гестации по 7 день жизни младенца) энцефалопатия гипоксической этиологии диагностируется у 5% появившихся на свет грудничков.
Повреждения структур мозга составляют 60% в общей массе болезней, поражающих нервную систему и выявленных в детском возрасте, чаще возникают как результат нарушения родового процесса. Последствия кислородного голодания мозга у новорожденных выражаются в развитии заболеваний – ДЦП, ММД (минимальная дисфункция мозга), эпилепсия.
В условиях гипоксии происходит нарушение метаболических процессов, в частности перекисного окисления липидных фракций (ПОЛ), что приводит к аккумуляции свободных радикалов, развитию гидроперекисии (преобразование липидов в первичные продукты ПОЛ с последующим повреждением липидного слоя клеточной мембраны). В результате повышается проницаемость мембран нейронов, возникает расстройство церебральной гемодинамики, протекающее по ишемическо-геморрагическому типу.
Разновидности гипоксии
Нарушение оксигенации (насыщение кислородом) крови коррелирует с гипоксией периферической и центральной формы. В первом случае в патогенезе участвуют патологические процессы, затрагивающие дыхательные пути и альвеолярный кровоток. Дисфункция дыхательного центра лежит в основе патогенеза центральной гипоксии. Этиологические факторы, провоцирующие возникновение периферической гипоксии:
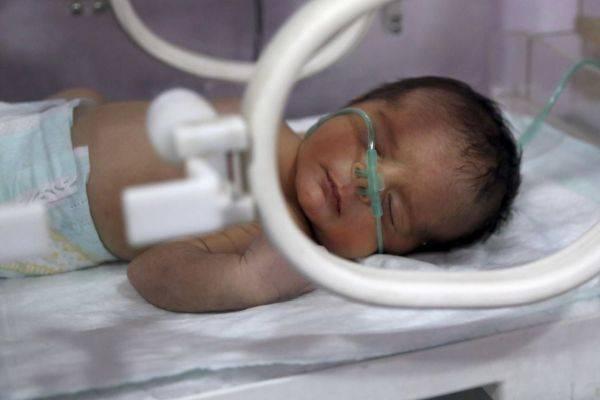
- Респираторный дистресс-синдром (тяжелое расстройство дыхания, выявляется преимущественно у недоношенных новорожденных, что связано с недоразвитием, незрелостью легких).
- Аспирация (попадание в дыхательные пути плода) околоплодных вод.
- Пневмоторакс (присутствие воздуха в плевральной полости легкого).
- Бронхолегочная дисплазия (заболевание морфологически незрелых легких, выявляется преимущественно у недоношенных младенцев).
- Врожденные аномалии дыхательной системы.
Центральная гипоксия головного мозга у детей развивается вследствие артериальной гипотонии, артериальной гипертензии, анемии матери. Спровоцировать гипоксическую энцефалопатию могут пороки формирования мозга плода и плацентарная недостаточность (нарушение функций плаценты).
Различают хроническую (перинатальную) и острую (родовую) формы. Первая коррелирует с нарушением течения беременности, вторая связана с травмами и патологиями, возникшими в результате родовой деятельности.
Причины возникновения
Гипоксия, которая является причиной повреждения головного мозга у новорожденных, отличается полиморфной этиологией. Возникновение патологии коррелирует со многими влияющими факторами:
- Возраст матери младше 20 лет или старше 40 лет.
- Отслаивание плаценты до наступления срока родов.
- Предлежание (неправильное расположение) плаценты.
- Преэклампсия (осложнение беременности в III триместре, связанное с изменением у матери показателей артериального давления, которые повышаются резко или медленно и равномерно).
- Нарушение срока родов (преждевременные, поздние).
- Попадание мекония (первые фекалии младенца) в околоплодные воды.
- Патологии сердца плода (брадикардия, тахикардия, приглушенные тона).
- Многоплодная беременность.
- Заболевания, перенесенные матерью в период гестации.
- Сахарный диабет у матери в анамнезе.
- Бесконтрольный прием матерью фармацевтических препаратов в период вынашивания плода.
Плацентарная недостаточность считается основной причиной гипоксии в антенатальном (предродовом) периоде. Патология протекает на фоне ухудшения всасываемости питательных, необходимых для развития плода веществ, поступающих через плаценту, и вследствие нарушения процесса их усвоения. Сопровождается нарушением газообмена (кислород и углекислота).
Состояние проявляется задержкой формирования плода, гипотрофией (белково-энергетическая недостаточность), недоразвитостью легких, дефицитом легочного сурфактанта (смесь поверхностно-активных веществ, выстилающих внутреннюю поверхность легочных альвеол). Перечисленные патологические процессы влекут серьезные заболевания у новорожденных детей – ДЦП, эпилепсию, синдромы повышенной активности и дефицита внимания, а также социальной дезадаптации.
Компенсация сахарного диабета у беременных женщин является профилактикой возникновения у ребенка дыхательного дистресс-синдрома и обусловленной им энцефалопатии гипоксической этиологии. Механизм кислородного голодания в этом случае связан с гиперинсулизмом плода, который формируется как ответная реакция на гипергликемию матери. Инсулин замедляет синтез лецитина, который является основным компонентом сурфактанта.
Причины гипоксических изменений, которые произошли в тканях головного мозга новорожденных в ходе родов, чаще связаны с нарушением родовой деятельности – расстройством сократительной функции матки (10-15% всех случаев), нарушением раскрытия шейки матки. Другие причины родовой формы гипоксии:
- Неправильное (ножное, ягодичное) предлежание плода.
- Затяжные или стремительные роды.
- Стимуляция родовой деятельности препаратом Окситоцин.
- Использование дополнительных средств (акушерские щипцы, выполнение кесарева сечения) для родоразрешения.
- Разрыв матки.
Кислородное голодание мозга у появившегося на свет ребенка может появиться как следствие гемолитической болезни, инфекционного внутриутробного заболевания, кровоизлияния в мозговое вещество и надпочечники. В неонатальный (с момента рождения по 28 день жизни) период в патогенезе кислородного голодания важную роль играют выявленные у младенца сердечная недостаточность, кардиомиопатия и другие патологии сердечно-сосудистой системы, недостаточность надпочечников.
Диагностика
Инструментальные методы включают нейросонографию, электроэнцефалографию, рентгенографию легких (при подозрении на врожденную пневмонию и другие воспалительные процессы в органах дыхания). Особенно подвержены повреждениям мозговой ткани вследствие кислородного голодания младенцы с дефицитом массы тела, выявленной гипогликемией (пониженный уровень глюкозы) и недостатком запасов гликогена. Состояние новорожденного оценивается по шкале Апгар. Использующиеся критерии:
- Внешний вид и состояние кожных покровов (цвет).
- Частота сокращений сердца (пульс).
- Мимика (сокращение мышц лица), которая возникает как ответная реакция на раздражающий фактор.
- Моторная активность, тонус мускулов.
- Параметры дыхания.
По каждому критерию оценка состояния осуществляется по шкале от 0 до 2 баллов, затем все баллы суммируются. Тестирование проводится на 1 и 5 минутах после появления ребенка на свет. Оценка 8-10 баллов указывает на удовлетворительное состояние малыша. Оценка 6-7 баллов (1 минута) свидетельствует о гипоксическом поражении легкой степени, 4-5 баллов (1 минута) является признаком централизации кровообращения, которое сопровождается нарушением в работе органов, в первую очередь ЦНС.
Оценка 0-3 балла указывает на тяжелую степень кислородного голодания, которое протекает с грубыми сбоями в работе органов и систем. Возможно развитие коматозного или шокового состояния. Младенец начинает слышать с первых минут жизни, тестирование в соответствии с критериями шкалы Апгар позволяет выявить его чувствительность к внешним раздражителям: когда врач вставляет катетер в носовые ходы ребенка, здоровый малыш начинает чихать.
Симптомы
Выделяют 3 периода развития перинатальной энцефалопатии, которая возникает в результате кислородного голодания – острый (с момента появления на свет до 30 дней жизни), восстановительный (с 30 дней до 1-2-годовалого возраста), исход. Клиническая картина различается в соответствии с периодом течения. Острый период сопровождается синдромами:
- Усиленной нервно-рефлекторной возбудимости. Симптомокомплекс характерен для состояния 6-7 баллов (Апгар). Типичны признаки: усиление спонтанной моторной активности, расстройство сна (беспокойный, прерывающийся), трудности при засыпании, удлинение фазы бодрствования в структуре суток, немотивированный плач. Параллельно наблюдается дистония (патологическое сокращение) мышц, усиление безусловных рефлексов, тремор (дрожание) конечностей и зоны подбородка.
- Судорожный. Типичные признаки: судороги тонико-клонического или тонического типа. Параллельно возникают клонические судороги местной локализации и гемиконвульсии (конвульсии в одной половине тела).
- Гипертензионно-гидроцефальный. Синдром характерен для состояния 4-6 баллов (Апгар). Проявляется увеличением диаметра черепа, расхождением швов костных структур черепа, выбуханием родничка. Типичные признаки: горизонтальный нистагм, косоглазие сходящего типа, мышечная дистония, вздрагивания, непроизвольный рефлекс Моро (разведение рук в стороны). Часто наблюдаются признаки: расстройство сна, цианоз (синюшный оттенок кожи).
- Угнетения. Синдром характерен для состояния 4-6 баллов (Апгар). Типичные признаки: вялость, гиподинамия (ослабление мышечной деятельности), ослабление моторной активности, гипорефлексия (слабые врожденные рефлексы).
- Коматозный. Синдром характерен для состояния 1-4 балла (Апгар). Типичные признаки: вялость и адинамия (отсутствие двигательной активности), гипотония и атония (отсутствие тонуса) мышц. Рефлексы не проявляются, зрачки не реагируют на световой раздражитель, реакция на болевое воздействие отсутствует. Наблюдаются признаки: нарушение дыхательного ритма, появление апноэ (остановки дыхания), приглушенные тона сердца, понижение значений артериального давления.
Чаще появляется несколько синдромов в комплексе. Острый период характеризуется преобладанием общемозговых нарушений без четко разграниченной очаговой симптоматики. У недоношенных малышей усиленная нервно-рефлекторная возбудимость может указывать на пониженные показатели судорожной готовности, что ассоциируется с активизацией судорожных, эпилептиформных процессов.
Методы лечения
При выявлении у детей симптомов, характерных для острого периода кислородного голодания мозга, лечение включает организацию вентиляции легких и коррекцию нарушений, спровоцированных респираторным дистресс-синдромом. Основные направления терапии:
- Антиоксидантная (уменьшение последствий окислительного стресса).
- Метаболическая (регуляция обменных процессов).
- Сосудистая (укрепление и регуляция тонуса сосудистой стенки).
- Дегидратационная (повышение осмотического давления плазмы крови).
- Противосудорожная, противоэпилептическая.
Терапия направлена на нормализацию гомеостаза (саморегуляция) и обмена веществ, улучшение метаболизма в тканях, уменьшение проницаемости стенок элементов кровеносной системы. Массаж, лечебная гимнастика и другие оздоровительные процедуры показаны в восстановительный период. Параллельно проводится симптоматическое лечение, направленное на устранение неврологического дефицита.
Хирургическая операция (вентрикулярное шунтирование) проводится, если диагностированы кровоизлияния перивентрикулярной (вблизи желудочковой системы) локализации в сочетании с гидроцефалией постгеморрагического генеза. Около 20% детей после корректного лечения выздоравливают полностью.
Возможные последствия
Последствия для мозга при гипоксии у новорожденного зависят от длительности патологического процесса. У младенцев количество используемого мозгом кислорода составляет около 50% (у взрослых людей – около 20%). Большое количество поступающего кислорода обуславливает ускоренный метаболизм процессов окисления.
В зависимости от периода кислородного голодания, изменения в мозговом веществе могут выражаться в виде локального отека (легкая форма) или некротического поражения ткани (тяжелая форма), сопровождающегося геморрагическим пропитыванием (кровоизлияние). Если гипоксия сочетается с ишемией, происходит поражение чувствительных к дефициту кислорода участков (корковые структуры, зрительный бугор, мозжечок) с образованием очагов некроза. Различают степени патологического процесса:
- 1-я степень. Отечно-геморрагическая.
- 2-я степень. Глиоз энцефалического генеза.
- 3-я степень. Лейкомаляция (некротические изменения в белом веществе).
- 4-я степень. Лейкомаляция, сопровождающаяся кровоизлиянием.
Церебральная гипоксия 1 и 2 степени у новорожденного является курабельной (излечимой). Гипоксическое поражение мозговых структур 3 и 4 степени протекает на фоне необратимой гибели нейронов с вытекающими последствиями – дисфункция мозга, появление выраженной неврологической симптоматики, риск летального исхода. Гипоксия у новорожденных находится на 2 месте после недоношенности в общей структуре причин перинатальной смертности.
Гипоксическая энцефалопатия, развивающаяся в перинатальный период – патология, которая грозит серьезными последствиями. Регулярное посещение врача в период беременности и соблюдение врачебных рекомендаций снижают риск развития патологических процессов. Корректное лечение новорожденного поможет уменьшить негативное влияние дефицита кислорода на мозг.